Thuốc Cresemba 100mg Pfizer điều trị nhiễm nấm Aspergillus xâm lấn và nhiễm nấm Mucorales (2 vỉ x 7 viên)















| Mô tả |
CRESEMBA® 100mg là sản phẩm được phân phối bởi Công ty TNHH Pfizer, có thành phần chính là Isavuconazole. Đây là thuốc dùng để điều trị nhiễm nấm Aspergillus xâm lấn và nhiễm nấm Mucorales ở bệnh nhân không thích hợp với amphotericin B. |
| Danh mục | Thuốc |
| Thương hiệu |
 Pfizer
Pfizer |
| Số đăng ký | 760110441723 |
| Dạng bào chế | Viên nang cứng |
| Quy cách | Hộp 2 Vỉ x 7 Viên |
| Thành phần | Isavuconazole |
| Nhà sản xuất | Thụy Sĩ |
| Nước sản xuất | Mỹ |
| Thuốc cần kê toa | Có |
Thành phần của Thuốc Cresemba 100mg
| Thông tin thành phần | Hàm lượng |
|---|---|
| Isavuconazole | 100mg |
Công dụng của Thuốc Cresemba 100mg
Chỉ định
Thuốc CRESEMBA® 100mg được chỉ định dùng trong các trường hợp sau:
- Nhiễm nấm Aspergillus xâm lấn.
- Nhiễm nấm Mucorales ở bệnh nhân không thích hợp với amphotericin B.
Cần xem thêm hướng dẫn chính thức về việc sử dụng thích hợp các thuốc kháng nấm.
Dược lực học
Nhóm dược lý: Thuốc kháng nấm dùng toàn thân, dẫn xuất triazole.
Mã ATC: J02AC05.
Cơ chế tác dụng
Isavuconazole là phần phân tử có hoạt tính được hình thành sau khi dùng isavuconazonium sulfate qua đường uống hoặc qua tĩnh mạch.
Isavuconazole thể hiện tác dụng kháng nấm bằng cách ngăn chặn sự tổng hợp ergosterol, một thành phần chính của màng tế bào nấm, thông qua ức chế enzym phụ thuộc cytochrome P-450 lanosterol 14-alpha-demethylase, chịu trách nhiệm chuyển đổi lanosterol thành ergosterol. Điều này dẫn đến sự tích lũy các tiền chất sterol đã methyl hóa và cạn kiệt ergosterol bên trong màng tế bào, từ đó làm suy yếu cấu trúc và chức năng của màng tế bào nấm.
Vi sinh
Trong các mô hình động vật bị nhiễm nấm Aspergillus lan tỏa và ở phổi, thông số dược lực học (Pharmacodynamic, PD) quan trọng trong tính hiệu quả là mức độ phơi nhiễm chia cho nồng độ ức chế tối thiểu (Minimum Inhibitory Concentration - MIC) (AUC/MIC).
Không thể thiết lập mối tương quan rõ ràng giữa MIC in vitro và đáp ứng lâm sàng đối với các loài khác nhau (Aspergillus và Mucorales).
Nồng độ của isavuconazole cần để ức chế các loài Aspergillus và các giống/loài trong bộ Mucorales in vitro rất khác nhau. Nói chung, nồng độ isavuconazole cần để ức chế Mucorales cao hơn nồng độ cần đề ức chế phần lớn các loài Aspergillus.
Hiệu quả lâm sàng đã được chứng minh đối với các loài Aspergillus sau: Aspergillus fumigatus, A. flavus, A. niger, và A. terreus.
Các cơ chế kháng thuốc
Hiện tượng giảm độ nhạy với các thuốc kháng nấm triazole đã thấy có liên quan đến các đột biến trong các gen cyp51A và cyp51B của nấm mã hóa protein đích là lanosterol 14-alpha-demethylase tham gia vào quá trình sinh tổng hợp ergosterol. Các chủng nấm giảm độ nhạy in vitro với isavuconazole đã được báo cáo, và không thể loại trừ khả năng kháng chéo với voriconazole và các thuốc kháng nấm nhóm triazole khác.
Điểm gãy
Điểm gãy MIC EUCAST đã được xác định cho các loài sau (S nhạy; R kháng):
- Aspergillus fumigatus: S ≤ 1 mg/L, R > 1 mg/L;
- Aspergillus nidulans: S ≤ 0,25 mg/L, R > 0,25 mg/L;
- Aspergillus terreus: S ≤ 1 mg/L, R > 1 mg/L.
Hiện không đủ dữ liệu đề thiết lập điểm gãy lâm sàng cho các loài Aspergillus.
Tính hiệu quả và tính an toàn lâm sàng
Điều trị nhiễm nấm Aspergillus xâm lấn
Tính an toàn và hiệu quả của isavuconazole trong điều trị bệnh nhân bị nhiễm nấm xâm lấn đã được đánh giá trong một nghiên cứu lâm sàng mù đôi, có đối chứng với thuốc thật ở 516 bệnh nhân bị bệnh nấm xâm lấn do các loài Aspergillus hoặc nấm sợi khác gây ra. Trong nhóm phân tích theo phân bố ngẫu nhiên ban đầu (ITT), 258 bệnh nhân dùng isavuconazole và 258 bệnh nhân dùng voriconazole. Isavuconazole được dùng qua tĩnh mạch (tương đương với 200 mg isavuconazole) mỗi 8 giờ trong 48 giờ đầu tiên, sau đó là một liều mỗi ngày qua tĩnh mạch hoặc qua đường uống (tương đương với 200 mg isavuconazole). Thời gian điều trị tối đa được xác định theo phác đồ là 84 ngày. Thời gian điều trị trung vị là 45 ngày.
Đáp ứng tổng thể ở cuối quá trình điều trị (End-Of-Treatment - EOT) trong quần thể myITT (các bệnh nhân có bằng chứng và có thể nhiễm nấm Aspergillus xâm lấn dựa trên nghiên cứu tế bào, nghiên cứu mô, nuôi cấy hoặc xét nghiệm galactomannan) đã được đánh giá bởi một Ủy ban đánh giá dữ liệu độc lập không biết về nghiên cứu. Quần thể myITT bao gồm 123 bệnh nhân dùng isavuconazole và 108 bệnh nhân dùng voriconazole. Đáp ứng tổng thể trong quần thể này là n=43 (35%) đối với isavuconazole và n=42 (38,9%) đối với voriconazole. Chênh lệch điều trị đã điều chỉnh (voriconazole - isavuconazole) là 4,0% (khoảng tin cậy 95%: - 7,9; 15,9).
Tỷ lệ tử vong do tất cả các nguyên nhân ở ngày 42 trong quần thể này là 18,7% đối với isavuconazole và 22,2% đối với voriconazole. Chênh lệch điều trị đã điều chỉnh (isavuconazole - voriconazole) là -2,7% (khoảng tin cậy 95%: - 12,9; 7,5).
Điều trị nhiễm nấm Mucorales
Trong một nghiên cứu nhãn mở, không có đối chứng, 37 bệnh nhân có bằng chứng hoặc có thể nhiễm nấm Mucorales đã dùng isavuconazole với cùng phác đồ liều giống như phác đồ dùng để điều trị nhiễm nấm Aspergillus xâm lấn. Thời gian điều trị trung vị là 84 ngày cho toàn bộ quần thể bệnh nhân nhiễm nấm Mucorales, và 102 ngày cho 21 bệnh nhân chưa từng được điều trị nhiễm nấm Mucorales trước đó. Đối với các bệnh nhân có bằng chứng hoặc có thể nhiễm nấm Mucorales như được xác định bởi Ủy ban đánh giá dữ liệu (Data Review Committee - DRC) độc lập, tỷ lệ tử vong do tất cả các nguyên nhân tại ngày 84 là 43,2% (16/37) với toàn thể quần thể bệnh nhân, 42,9% (9/21) với những bệnh nhân nhiễm nấm Mucorales dùng isavuconazole làm biện pháp điều trị ban đầu, và 43,8% (7/16) với những bệnh nhân nhiễm nấm Mucorales dùng isavuconazole là người đã bị kháng thuốc, không dung nạp liệu pháp kháng nấm trước đó (chủ yếu là các phương pháp điều trị sử dụng amphotericin B). Tỷ lệ thành công tổng thể theo đánh giá của DRC vào EOT là 11/35 (31,4%), với 5 bệnh nhân được xem là khỏi hoàn toàn và 6 bệnh nhân khỏi một phần. Đã quan sát thấy đáp ứng ổn định ở thêm 10/35 bệnh nhân (28,6%). Ở 9 bệnh nhân nhiễm nấm Mucorales do các loài Rhizopus, 4 bệnh nhân biểu hiện đáp ứng thuận lợi cho isavuconazole. Ở 5 bệnh nhân nhiễm nấm Mucorales do các loài Rhizomucor, không quan sát thấy đáp ứng thuận lợi. Có rất ít kinh nghiệm lâm sàng ở các loài khác (các loài Lichtheimia n=2, các loài Cunninghamella n=1, Actinomucor elegans n=1).
Dược động học
Isavuconazonium sulfate là một tiền dược tan trong nước có thể dùng dưới dạng truyền tĩnh mạch hoặc uống dưới dạng viên nang cứng. Sau khi dùng thuốc, isavuconazonium sulfate nhanh chóng bị thủy phân bởi các esterase trong huyết tương thành phần phân tử có hoạt tính là isavuconazole; nồng độ trong huyết tương của tiền dược rất thấp, và chỉ phát hiện được trong một thời gian ngắn sau khi dùng thuốc qua tĩnh mạch.
Hấp thu
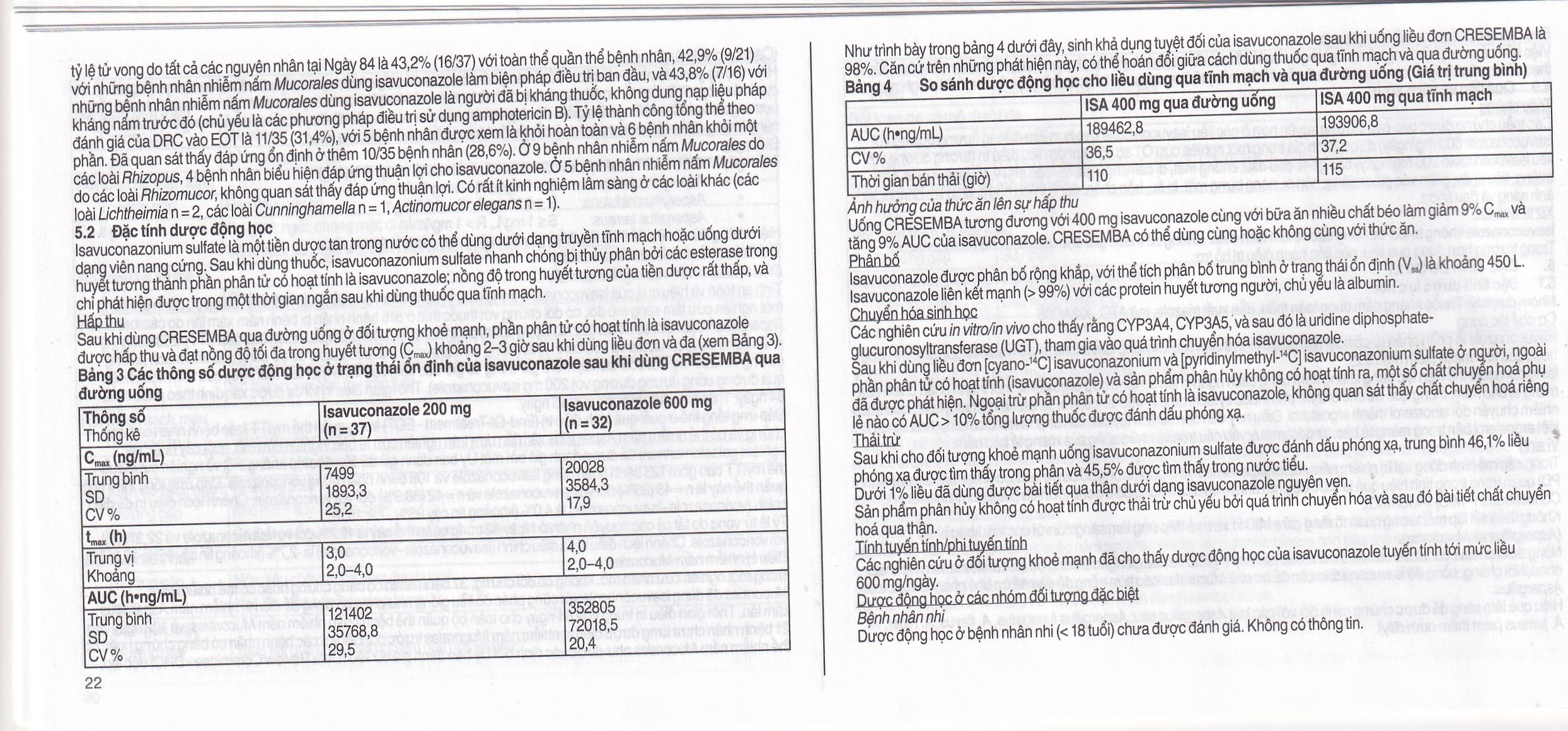
Sau khi dùng CRESEMBA® qua đường uống ở đối tượng khỏe mạnh, phần phân tử có hoạt tính là isavuconazole được hấp thu và đạt nồng độ tối đa trong huyết tương (Cmax) khoảng 2 - 3 giờ sau khi dùng liều đơn và đa.
Thông số Thống kê | Isavuconazole 200 mg (n=37) | Isavuconazole 600 mg (n=32) |
|---|---|---|
| Cmax (ng/mL) | ||
Trung bình SD CV% | 7499 1893,3 25,2 | 20028 3584,3 17,9 |
| tmax (h) | ||
Trung vị Khoảng | 3,0 2,0 - 4,0 | 4,0 2,0 - 4,0 |
| AUC (h•ng/mL) | ||
Trung bình SD CV% | 121402 35768,8 29,5 | 352805 72018,5 20,4 |
Như trình bày trong bảng dưới đây, sinh khả dụng tuyệt đối của isavuconazole sau khi uống liều đơn CRESEMBA® là 98%. Căn cứ trên những phát hiện này, có thể hoán đổi giữa cách dùng thuốc qua tĩnh mạch và qua đường uống.
| ISA 400 mg qua đường uống | ISA 400 mg qua tĩnh mạch | |
|---|---|---|
| AUC (h•ng/mL) | 189462,8 | 193906,8 |
| CV% | 36,5 | 37,2 |
| Thời gian bán thải (giờ) | 110 | 115 |
Ảnh hưởng của thức ăn lên sự hấp thu
Uống CRESEMBA® tương đương với 400 mg isavuconazole cùng với bữa ăn nhiều chất béo làm giảm 9% Cmax và tăng 9% AUC của isavuconazole. CRESEMBA® có thể dùng cùng hoặc không cùng với thức ăn.
Phân bố
Isavuconazole được phân bố rộng khắp, với thể tích phân bố trung bình ở trạng thái ổn định (VSS) là khoảng 450 L. Isavuconazole liên kết mạnh (> 99%) với các protein huyết tương người, chủ yếu là albumin.
Chuyển hóa sinh học
Các nghiên cứu in vitro/in vivo cho thấy rằng CYP3A4, CYP3A5, và sau đó là uridine diphosphate-glucuronosyltransferase (UGT), tham gia vào quá trình chuyển hóa isavuconazole.
Sau khi dùng liều đơn [cyano-14C] isavuconazonium và [pyridinylmethyl-14C] isavuconazonium sulfate ở người, ngoài phần phân tử có hoạt tính (isavuconazole) và sản phẩm phân hủy không có hoạt tính ra, một số chất chuyển hóa phụ đã được phát hiện. Ngoại trừ phần phân tử có hoạt tính là isavuconazole, không quan sát thấy chất chuyển hoá riêng lẻ nào có AUC > 10% tổng lượng thuốc được đánh dấu phóng xạ.
Thải trừ
Sau khi cho đối tượng khỏe mạnh uống isavuconazonium sulfate được đánh dấu phóng xạ, trung bình 46,1% liều phóng xạ được tìm thấy trong phân và 45,5% được tìm thấy trong nước tiểu.
Dưới 1% liều đã dùng được bài tiết qua thận dưới dạng isavuconazole nguyên vẹn.
Sản phẩm phân hủy không có hoạt tính được thải trừ chủ yếu bởi quá trình chuyển hóa và sau đó bài tiết chất chuyển hóa qua thận.
Tính tuyến tính/phi tuyến tính
Các nghiên cứu ở đối tượng khoẻ mạnh đã cho thấy dược động học của isavuconazole tuyến tính tới mức liều 600 mg/ngày.
Dược động học ở các nhóm đối tượng đặc biệt
Bệnh nhân nhi
Dược động học ở bệnh nhân nhi (< 18 tuổi) chưa được đánh giá. Không có thông tin.
Suy giảm chức năng thận
Không quan sát thấy thay đổi liên quan lâm sàng nào về tổng Cmax và AUC của isavuconazole ở các đối tượng suy giảm chức năng thận nhẹ, vừa hoặc nặng so với các đối tượng có chức năng thận bình thường. Trong số 403 bệnh nhân dùng isavuconazole trong các nghiên cứu pha ba, 79 (20%) bệnh nhân có tốc độ lọc cầu thận (Glomerular Filtration Rate - GFR) ước tính thấp hơn 60 mL/phút/1,73 m2. Không cần điều chỉnh liều ở bệnh nhân suy giảm chức năng thận, bao gồm cả bệnh nhân suy thận thời kỳ cuối. Isavuconazole không dễ thẩm tách.
Suy giảm chức năng gan
Sau khi dùng liều đơn 100 mg isavuconazole cho 32 bệnh nhân suy gan nhẹ (Child-Pugh loại A) và 32 bệnh nhân suy gan vừa (Child-Pugh loại B) (16 bệnh nhân dùng đường tĩnh mạch và 16 bệnh nhân dùng đường uống ở mỗi loại Child-Pugh), mức độ phơi nhiễm toàn thân (AUC) trung bình theo phương pháp bình phương tối thiểu tăng 64% trong nhóm Child-Pugh loại A, và 84% trong nhóm Child-Pugh loại B, so với 32 đối tượng khỏe mạnh cùng độ tuổi và cân nặng có chức năng gan bình thường. Nồng độ trung bình trong huyết tương (Cmax) thấp hơn 2% trong nhóm Child-Pugh loại A và thấp hơn 30% trong nhóm Child-Pugh loại B. Đánh giá dược động học nhóm đối tượng của isavuconazole ở các đối tượng khỏe mạnh và bệnh nhân rối loạn chức năng gan nhẹ hoặc vừa cho thấy rằng các nhóm đối tượng suy giảm chức năng gan nhẹ và vừa có giá trị độ thanh thải (Clearance - CL) isavuconazole thấp hơn lần lượt là 40% và 48% so với nhóm đối tượng khỏe mạnh.
Không cần điều chỉnh liều ở bệnh nhân suy giảm chức năng gan nhẹ đến vừa.
Isavuconazole chưa được nghiên cứu ở bệnh nhân suy giảm chức năng gan nặng (Child-Pugh loại C). Không khuyến nghị sử dụng ở những bệnh nhân này trừ khi lợi ích tiềm năng được cân nhắc là lớn hơn nguy cơ.
Cách dùng Thuốc Cresemba 100mg
Cách dùng
Thuốc dạng viên nang dùng đường uống. Uống trọn viên thuốc với một ly nước cùng hoặc không cùng với thức ăn. Không nhai, nghiền, hòa tan hay mở viên thuốc.
Liều dùng CRESEMBA® 100mg
Liều tấn công (viên nang cứng):
Liều tấn công được khuyến nghị là 2 viên uống (tương đương với 200 mg isavuconazole) mỗi 8 giờ trong 48 giờ đầu tiên (tổng cộng 6 lần sử dụng).
Liều duy trì:
Liều duy trì được khuyến nghị là 2 viên uống (tương đương với 200 mg isavuconazole) ngày một lần, bắt đầu 12 đến 24 giờ sau liều tấn công cuối cùng.
Thời gian điều trị cần được quyết định theo đáp ứng lâm sàng.
Để điều trị dài hạn quá 6 tháng, cần phải cân nhắc cẩn thận cân bằng lợi ích/nguy cơ.
Chuyển sang truyền tĩnh mạch:
CRESEMBA® cũng được cung cấp dưới dạng bột pha dung dịch đậm đặc để pha dung dịch truyền có chứa 200 mg isavuconazole.
Trên cơ sở sinh khả dụng qua đường uống cao (98%), chuyển đổi giữa việc dùng qua tĩnh mạch và dùng qua đường uống là thích hợp khi có chỉ định lâm sàng.
Người cao tuổi
Không cần điều chỉnh liều cho bệnh nhân cao tuổi; tuy nhiên, kinh nghiệm lâm sàng trên bệnh nhân cao tuổi còn hạn chế.
Suy giảm chức năng thận
Không cần điều chỉnh liều ở bệnh nhân suy giảm chức năng thận, bao gồm bệnh nhân suy thận thời kỳ cuối.
Suy giảm chức năng gan
Không cần điều chỉnh liều ở bệnh nhân suy giảm chức năng gan nhẹ hoặc vừa (Child-Pugh loại A và B).
Isavuconazole chưa được nghiên cứu ở bệnh nhân suy giảm chức năng gan nặng (Child-Pugh loại C). Không khuyến nghị sử dụng ở những bệnh nhân này trừ khi lợi ích tiềm năng được cân nhắc là lớn hơn nguy cơ.
Bệnh nhân nhi
Tính hiệu quả và an toàn của CRESEMBA ở trẻ em dưới 18 tuổi chưa được thiết lập. Không có thông tin.
Lưu ý: Liều dùng trên chỉ mang tính chất tham khảo. Liều dùng cụ thể tùy thuộc vào thể trạng và mức độ diễn tiến của bệnh. Để có liều dùng phù hợp, bạn cần tham khảo ý kiến bác sĩ hoặc chuyên viên y tế.
Làm gì khi dùng quá liều?
Triệu chứng quá liều
Các triệu chứng được báo cáo thường xuyên hơn ở các liều isavuconazole cao hơn liều điều trị (tương đương với isavuconazole 600 mg/ngày) được đánh giá trong một nghiên cứu QT so với ở nhóm liều điều trị (tương đương với liều isavuconazole 200 mg/ngày) bao gồm: Đau đầu; chóng mặt, dị cảm, ngủ gà, rối loạn chú ý, rối loạn vị giác, khô miệng, tiêu chảy, giảm xúc giác miệng, nôn ói, nóng bừng mặt, lo âu, bồn chồn, đánh trống ngực, nhịp tim nhanh, sợ ánh sáng và đau khớp.
Xử trí quá liều
Isavuconazole không bị loại bỏ bằng cách thẩm tách máu. Không có thuốc giải độc đặc hiệu cho isavuconazole. Trong trường hợp dùng quá liều, nên tiến hành điều trị hỗ trợ.
Trong trường hợp khẩn cấp, hãy gọi ngay cho Trung tâm cấp cứu 115 hoặc đến trạm Y tế địa phương gần nhất.
Làm gì khi quên 1 liều?
Bổ sung liều ngay khi nhớ ra. Tuy nhiên, nếu thời gian giãn cách với liều tiếp theo quá ngắn thì bỏ qua liều đã quên và tiếp tục lịch dùng thuốc. Không dùng liều gấp đôi để bù cho liều đã bị bỏ lỡ.
Tác dụng phụ
Tóm tắt tính an toàn
Các phản ứng bất lợi liên quan đến điều trị thường gặp nhất là tăng kết quả chỉ số xét nghiệm về gan (7,9%), buồn nôn (7,4%), nôn (5,5%), khó thở (3,2%), đau bụng (2,7%), tiêu chảy (2,7%), phản ứng tại chỗ tiêm (2,2%), đau đầu (2,0%), giảm kali máu (1,7%) và phát ban (1,7%).
Các phản ứng bất lợi thường gặp nhất dẫn đến phải ngưng vĩnh viễn điều trị bằng isavuconazole là tình trạng lú lẫn (0,7%), suy thận cấp tính (0,7%), tăng bilirubin trong máu (0,5%), co giật (0,5%), khó thở (0,5%), động kinh (0,5%), suy hô hấp (0,5%) và nôn (0,5%).
Bảng danh sách các phản ứng bất lợi
Bảng dưới đây trình bày các phản ứng bất lợi khi sử dụng isavuconazole trong điều trị nhiễm nấm xâm lấn, theo phân loại hệ cơ quan và tần suất.
Tần suất của các phản ứng bất lợi được định nghĩa như sau: Rất thường gặp (≥ 1/10); thường gặp (≥ 1/100 đến < 1/10): và ít gặp (≥ 1/1000 đến < 1/100).
Trong mỗi nhóm tần suất, các phản ứng bất lợi được trình bày theo thứ tự mức độ nghiêm trọng giảm dần.
| Phân loại hệ cơ quan | Phản ứng bất lợi của thuốc |
|---|---|
| Rối loạn máu và hệ bạch huyết | |
| Ít gặp | Giảm bạch cầu trung tính; giảm tiểu cầu^; giảm ba dòng tế bào máu; giảm bạch cầu^; thiếu máu^ |
| Rối loạn hệ miễn dịch | |
| Ít gặp | Quá mẫn^ |
| Rối loạn chuyển hóa và dinh dưỡng | |
| Thường gặp | Giảm kali máu; chán ăn |
| Ít gặp | Giảm magnesi máu; hạ đường huyết; giảm albumin máu; suy dinh dưỡng^ |
| Rối loạn tâm thần | |
| Thường gặp | Mê sảng^# |
| Ít gặp | Trầm cảm; mất ngủ^ |
| Rối loạn hệ thần kinh | |
| Thường gặp | Đau đầu; ngủ gà |
| Ít gặp | Co giật^; ngất chóng mặt; dị cảm^ Bệnh não; tiền ngất xỉu; bệnh thần kinh ngoại biên; rối loạn vị giác |
| Rối loạn tai và mê lộ | |
| Ít gặp | Chóng mặt |
| Rối loạn tim | |
| Ít gặp | Rung nhĩ; nhịp tim nhanh; nhịp tim chậm^; đánh trống ngực Cuồng động nhĩ; rút ngắn khoảng QT trên điện tâm đồ; nhịp tim nhanh trên thất; ngoại tâm thu thất; ngoại tâm thu trên thất |
| Rối loạn mạch máu | |
| Thường gặp | Viêm tắc tĩnh mạch^ |
| Ít gặp | Trụy tuần hoàn; hạ huyết áp |
| Rối loạn hô hấp, ngực và trung thất | |
| Thường gặp | Khó thở^; suy hô hấp cấp^ |
| Ít gặp | Co thắt phế quản; thở nhanh; ho ra máu; chảy máu cam |
| Rối loạn tiêu hóa | |
| Thường gặp | Nôn; tiêu chảy; buồn nôn; đau bụng^ |
| Ít gặp | Khó tiêu; táo bón; chướng bụng |
| Rối loạn gan mật | |
| Thường gặp | Tăng kết quả chỉ số xét nghiệm hóa học về gan^# |
| Ít gặp | Gan lách phì đại; viêm gan |
| Rối loạn da và mô dưới da | |
| Thường gặp | Phát ban^; ngứa |
| Ít gặp | Đốm xuất huyết; rụng tóc; ban đỏ nhiễm sắc do thuốc; viêm da^ |
| Rối loạn cơ xương và mô liên kết | |
| Ít gặp | Đau lưng |
| Rối loạn thận và tiết niệu | |
| Thường gặp | Suy thận |
| Rối loạn chung và tình trạng tại nơi sử dụng thuốc | |
| Thường gặp | Đau ngực^; mệt mỏi |
| Ít gặp | Khó chịu; suy nhược |
^Biểu thị rằng đã nhóm các thuật ngữ được ưu tiên thích hợp vào một khái niệm y khoa duy nhất.
#Xem mục Mô tả các phản ứng bất lợi chọn lọc dưới đây.
Mô tả các phản ứng bất lợi chọn lọc
Mê sảng bao gồm các phản ứng của tình trạng lú lẫn.
Tăng kết quả chỉ số xét nghiệm hóa học về gan bao gồm các biến cố tăng alanine aminotransferase, tăng aspartate aminotransferase, tăng phosphatase kiềm trong máu, tăng bilirubin trong máu, tăng lactate dehydrogenase trong máu, tăng gamma-glutamyltransferase, tăng men gan, chức năng gan bất thường, kết quả xét nghiệm chức năng gan bất thường, và tăng transaminase.
Ảnh hưởng lên kết quả xét nghiệm
Trong một nghiên cứu lâm sàng mù đôi, chọn ngẫu nhiên, có đối chứng với thuốc thật ở 516 bệnh nhân bị bệnh nấm xâm lấn do các loài Aspergillus hoặc nấm sợi khác gây ra, tăng transaminase gan (alanine aminotransferase hoặc aspartate aminotransferase) > 3 x Giới hạn trên của trị số bình thường (Upper Limit of Normal, ULN) đã được báo cáo ở cuối quá trình điều trị nghiên cứu ở 4,4% bệnh nhân dùng isavuconazole. Đã gặp phải hiện tượng tăng rõ rệt transaminase gan > 10 x ULN ở 1,2% bệnh nhân dùng isavuconazole.
Hướng dẫn cách xử trí ADR:
Thông báo cho thầy thuốc các tác dụng không mong muốn gặp phải khi sử dụng thuốc.
Bảo quản
Hạn sử dụng: 30 tháng
Bảo quản nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp.
Để xa tầm tay trẻ em.