Thuốc Velsof 400mg/100mg Natco điều trị viêm gan virus C mạn tính ở người lớn (28 viên)











| Mô tả |
Thuốc Velsof là sản phẩm của NATCO PHARMA LIMITED, có thành phần chính là Sofosbuvir, Velpatasvir. Đây là thuốc được sử dụng để điều trị viêm gan virus C (HCV) mạn tính ở người lớn. |
| Danh mục | Thuốc |
| Thương hiệu |
 Natco
Natco |
| Số đăng ký | 890110776024 |
| Dạng bào chế | Viên nén bao phim |
| Quy cách | Hộp 28 Viên |
| Thành phần | Sofosbuvir, Velpatasvir |
| Nhà sản xuất | Ấn Độ |
| Nước sản xuất | Ấn Độ |
| Thuốc cần kê toa | Có |
Thành phần của Thuốc Velsof 400mg/100mg
| Thông tin thành phần | Hàm lượng |
|---|---|
| Sofosbuvir | 400mg |
| Velpatasvir | 100mg |
Công dụng của Thuốc Velsof 400mg/100mg
Chỉ định
Thuốc Velsof được chỉ định dùng trong các trường hợp sau:
- Viên nén sofosbuvirlvelpatasvir được chỉ định để điều trị viêm gan virus C (HCV) mạn tính ở người lớn.
Dược lực học
Nhóm thuốc: Thuốc kháng virus trực tiếp, mã ATC: J05AP55.
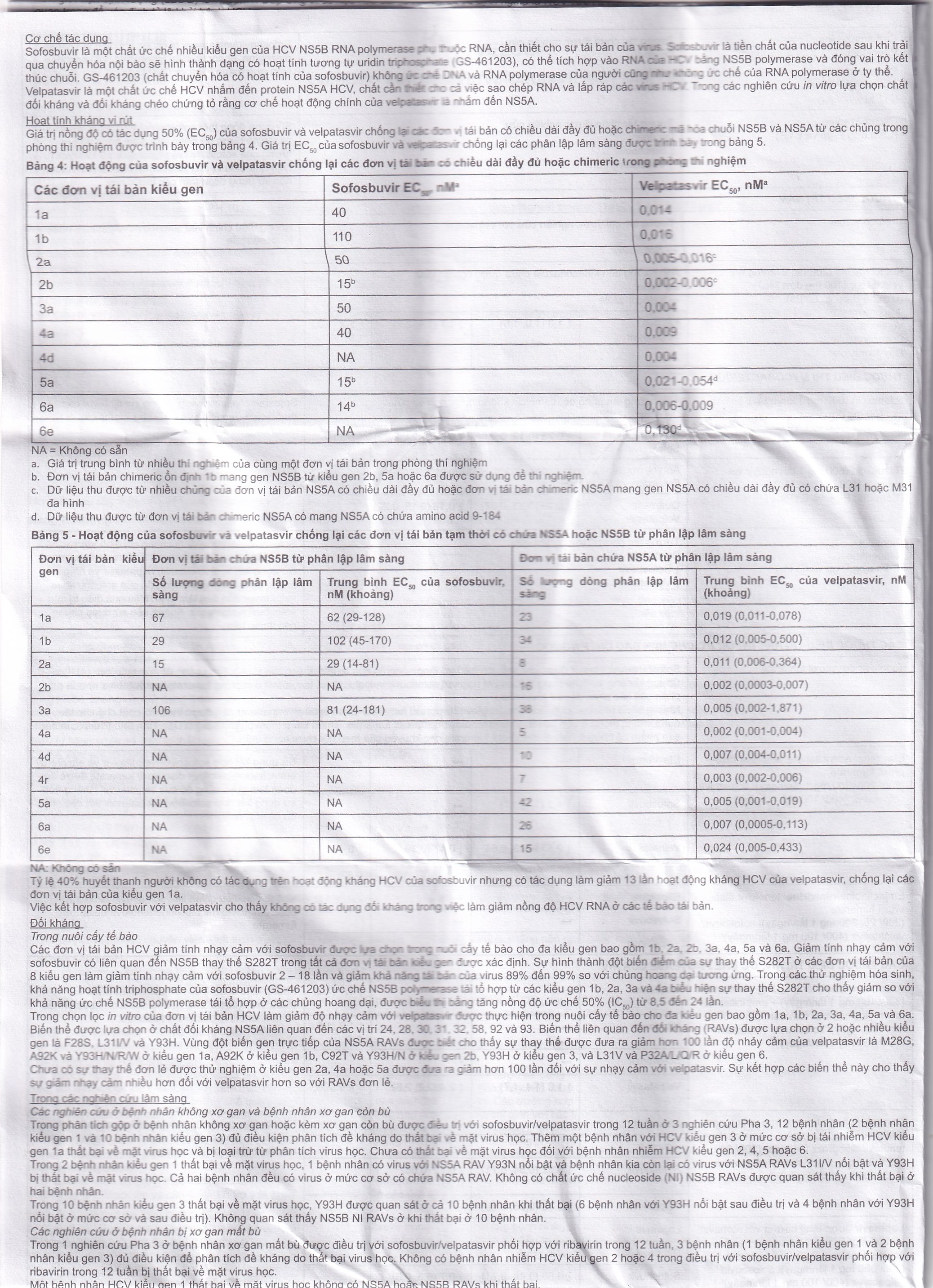
Cơ chế tác dụng
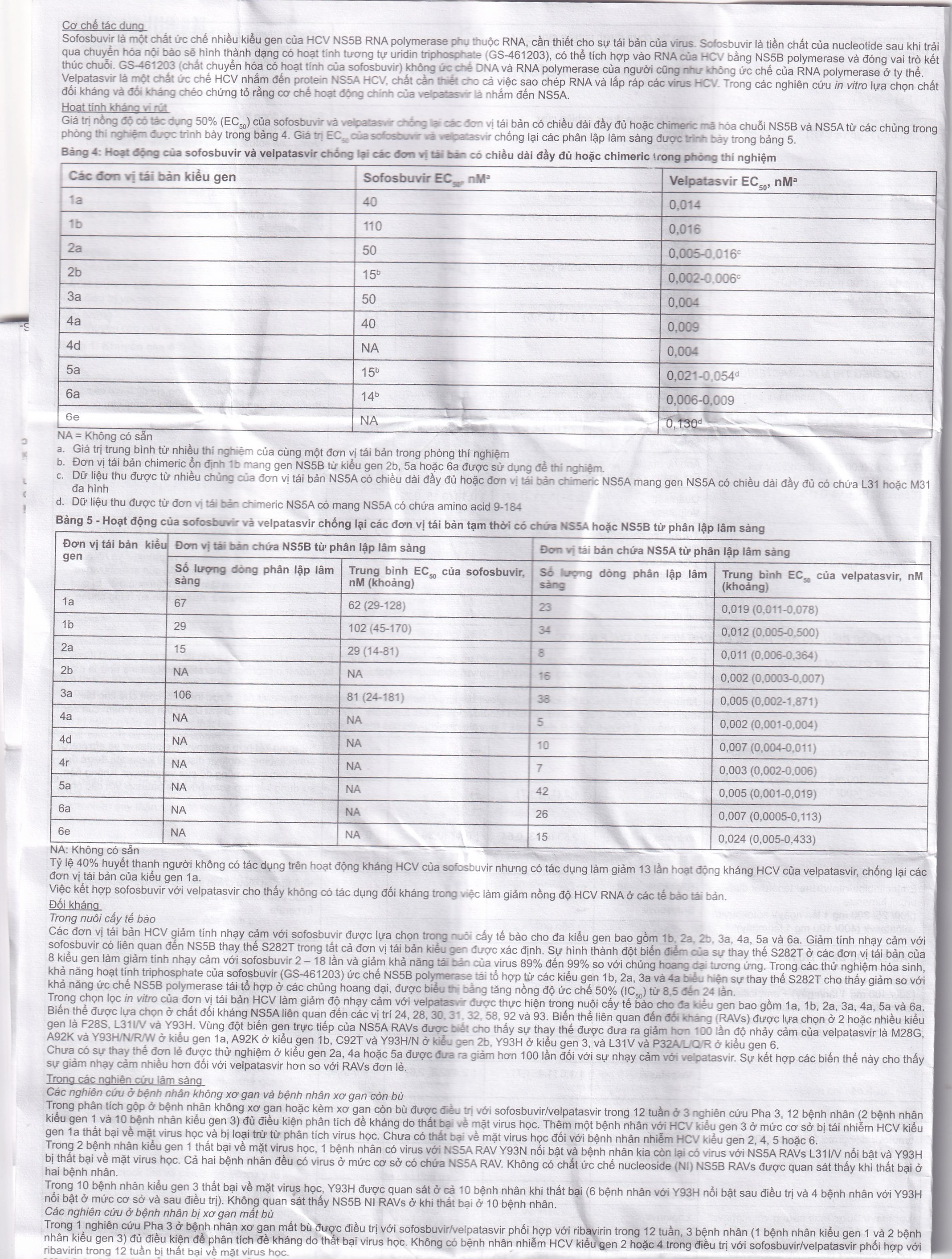
Sofosbuvir là một chất ức chế nhiều kiểu gen của HCV NS5B RNA polymerase tin, thuộc RNA, cần thiết cho sự tái bản của virus. Sainsbuvir là tiền chất của nucleotide sau khi trải qua chuyển hóa nội bào sẽ hình thành dạng có hoạt tính tương tự uridin triphosphate (GS-461203), có thể tích hợp vào RNA của bằng NS5B polymerase và đóng vai trò kết thúc chuỗi. GS-461203 (chất chuyển hóa có hoạt tính của sofosbuvir) không ức chế DNA và RNA polymerase của người cũng như không ức chế của RNA polymerase ở ty thể.
Velpatasvir là một chất ức chế HCV nhắm đến protein NS5A HCV, chất cần thiết cho cả việc sao chép RNA và lắp ráp các virus HPV. Trong các nghiên cứu in vitro lựa chọn chất đối kháng và đối kháng chéo chứng tỏ rằng cơ chế hoạt động chính của velpanature là nhằm đến NS5A.
Vui lòng xem thêm các thông tin về thuốc trong tờ hướng dẫn sử dụng thuốc đính kèm sản phẩm.
Dược động học
Hấp thu
Các đặc tính dược động học của sofosbuvir, chất chuyển hóa chủ yếu GS-331007 và velpatasvir đã được đánh giá ở người lớn khỏe mạnh và những người viêm gan C mạn tính.
Sau khi uống, sofosbuvir được hấp thu nhanh chóng và nồng độ đỉnh trung bình trong huyết tương đạt được khoảng sau 1 giờ. Nồng độ đỉnh trung bình trong huyết tương của GS-331007 được quan sát sau 3 giờ dùng thuốc. Nồng độ đỉnh trung bình trong huyết tương của Velpatasvir được quan sát sau 3 giờ dùng thuốc.
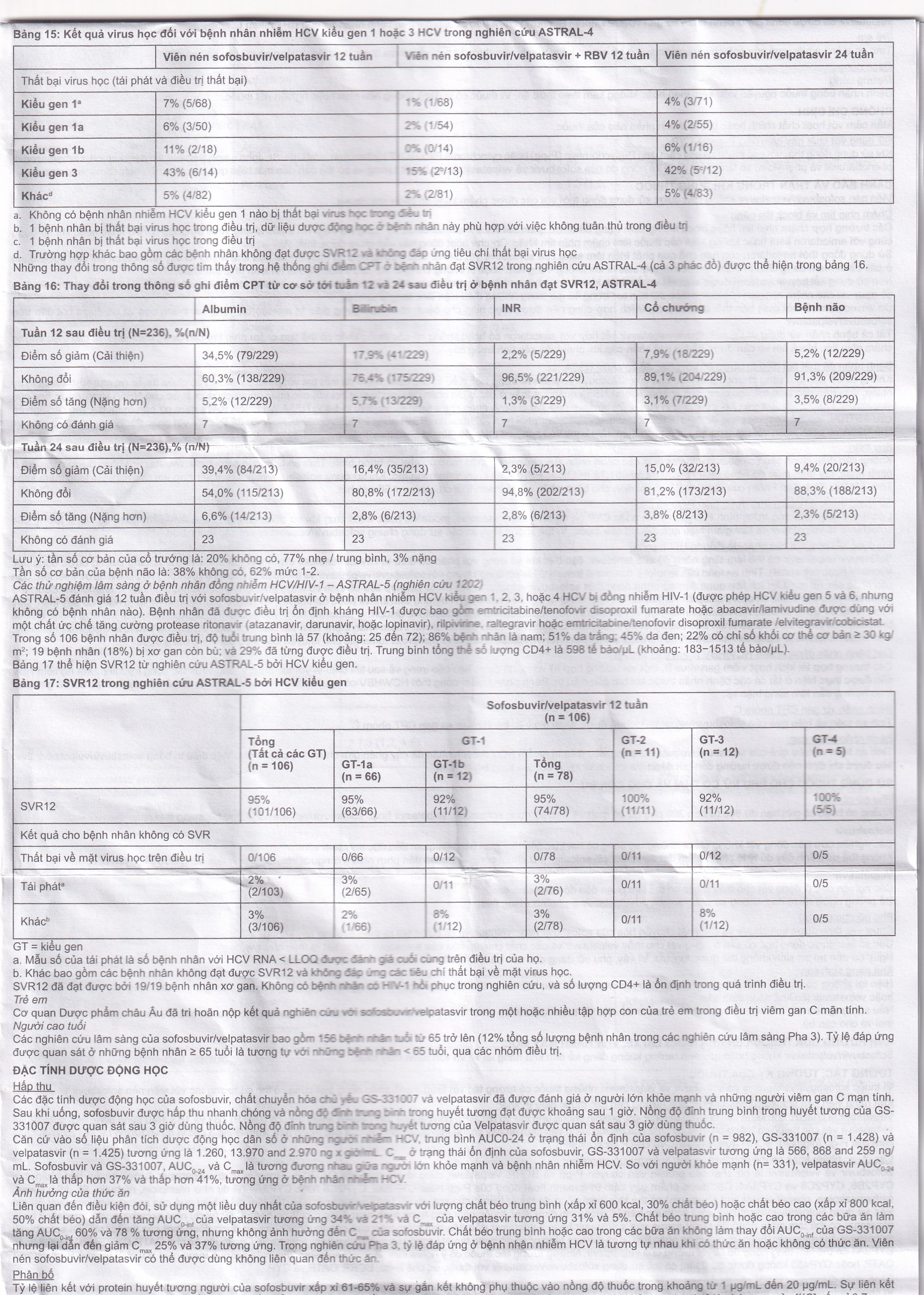
Căn cứ vào số liệu phân tích dược động học dân số ở những người nhiễm HCV, trung bình AUC0-24 ở trạng thái ổn định của sofosbuvir (n = 982), GS-331007 (n = 1.428) và velpatasvir (n = 1.425) tương ứng là 1.260, 13.970 and 2.970 ng x giờ/mL. Cmax ở trạng thái ổn định của sofosbuvir, GS-331007 và velpatasvir tương ứng là 566, 868 and 259 ng/mL. Sofosbuvir và GS-331007, AUC0-24 và Cmax là tương đương nhau giữa người lớn khỏe mạnh và bệnh nhân nhiễm HCV. So với người khỏe mạnh (n= 331), velpatasvir AUC0-24 và Cmax là thấp hơn 37% và thấp hơn 41%, tương ứng ở bệnh nhân nhiễm HCV.
Ảnh hưởng của thức ăn
Liên quan đến điều kiện đói, sử dụng một liều duy nhất của sofosbuvir/velpatasvir với lượng chất béo trung bình (xấp xỉ 600 kcal, 30% chất béo) hoặc chất béo cao (xấp xỉ 800 kcal, 50% chất béo) dẫn đến tăng AUC0-inf của velpatasvir tương ứng 34% và 21% và Cmax của velpatasvir tương ứng 31% và 5%. Chất béo trung bình hoặc cao trong các bữa ăn làm tăng AUC0-inf 60% và 78% tương ứng, nhưng không ảnh hưởng đến Cmax của sofosbuvir. Chất béo trung bình hoặc cao trong các bữa ăn không làm thay đổi AUC0-inf của GS-331007 nhưng lại dẫn đến giảm Cmax 25% và 37% tương ứng. Trong nghiên cứu Pha 3, tỷ lệ đáp ứng ở bệnh nhân nhiễm HCV là tương tự nhau khi có thức ăn hoặc không có thức ăn. Viên nén sofosbuvir/velpatasvir có thể được dùng không liên quan đến thức ăn.
Phân bố
Tỷ lệ liên kết với protein huyết tương người của sofosbuvir xấp xỉ 61-65% và sự gắn kết không phụ thuộc vào nồng độ thuốc trong khoảng từ 1 µg/mL đến 20 µg/mL. Sự liên kết của GS-331007 với protein trong huyết tương là tối thiểu. Sau khi dùng liều đơn 400mg của [14C]-sofosbuvir ở những người khỏe mạnh, và tỷ lệ phóng xạ của [C] xấp xỉ 0,7.
Tỷ lệ liên kết với protein huyết tương người của velpatasvir > 99,5% và sự gắn kết không phụ thuộc nồng độ thuốc trong khoảng từ 0,09 µg/ml đến 1,8 µg/ml. Sau khi dùng đơn liều 100 mg của [14C]-velpatasvir ở đối tượng khỏa mạnh, tỷ lệ của phóng xạ [14C] khoảng 0,52 và 0,67.
Chuyển hóa
Sofosbuvir được chuyển hóa rộng rãi ở gan để tạo thành các chất chuyển hóa có hoạt tính dược lý tương tự nucleosid triphosphat GS-461203. Quá trình chuyển hóa thành chất có hoạt tính liên quan đến quá trình thủy phân liên tiếp ester carboxyl moiety được xúc tác bởi cathepsin A người (CatA) hoặc carboxylesterase 1 (CES1) và sự phân cắt phosphoramidate bởi "histidine triad nucleotide-binding protein 1" (HINT1), tiếp theo là phosphoryl hóa bằng con đường sinh tổng hợp pyrimidine nucleotide. Quá trình dephosphoryl hóa là kết quả trong việc hình thành các chất chuyển hóa nucleosid GS-331007 nhưng không thể tái phosphoryl hóa hiệu quả và mất tác dụng chống HCV trong in vitro. Sofosbuvir và GS-331.007 không phải là cơ chất hoặc chất ức chế UGT1A1 hay enzym CYP3A4, CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, và CYP2D6. Sau khi uống liều đơn 400 mg [14C] -sofosbuvir, GS-331007 chiếm xấp xỉ > 90% lượng thuốc.
Velpatasvir là một cơ chất của CYP2B6, CYP2C8, và CYP3A4 với được chuyển hóa chậm. Sau một liều duy nhất 100 mg [14C] -velpatasvir, đa số (> 98%) phóng xạ trong huyết tương là thuốc mẹ. Các velpatasvir monohydroxylated và desmethylated là sản phẩm chuyển hóa trong huyết tương. Velpatasvir dạng không thay đổi và được bài tiết qua phân.
Thải trừ
Sau một liều uống duy nhất 400 mg [14C] -sofosbuvir, trung bình tổng thu hồi phóng xạ [14C] lớn hơn 92%, bao gồm xấp xỉ 80%, 14% và 2,5% được thu hồi tương ứng trong nước tiểu, phân và không khí thở ra. Thành phần chính của thuốc được thu hồi trong nước tiểu là GS-331007 (78%), trong khi 3,5% được thu hồi dưới dạng sofosbuvir. Dữ liệu này chỉ ra rằng đường thải trừ chính cho GS-331007 là được bài tiết ở thận. Thời gian bán thải cuối trung bình của sofosbuvir và GS-331007 sau khi dùng sofosbuvinive patasvir tương ứng là 0,5 và 25 giờ.
Sau một liều uống duy nhất 100 mg [14C] - velpatasvir, trung bình tổng thu hồi phóng xạ [14C] là 95%, bao gồm xấp xỉ 94% và 0,4% tương ứng được thu hồi qua phân và nước tiểu.
Velpatasvir dạng không chuyển hóa là thành phần chính có trong phần với trung bình lên tới 77% liều sử dụng, sau đó là monohydroxylated velpatasvir (5.9%) và desmethylated velpatasvir (3,0%). Những dữ liệu này cho thấy rằng velpatasvir được bài tiết qua đường mật là chủ yếu. Trung bình thời gian bán thải cuối của velpatasvir sau khi sử dụng viên nén sofosbuvir/velpatasvir xấp xỉ 15 giờ.
Độ tuyến tính/phi tuyến tính
AUC của velpatasvir tăng trong khoảng liều từ 25mg tới 100mg. AUC của sofosbuvir and GS-331007 tăng trong khoảng liều từ 200mg đến 1.200mg.
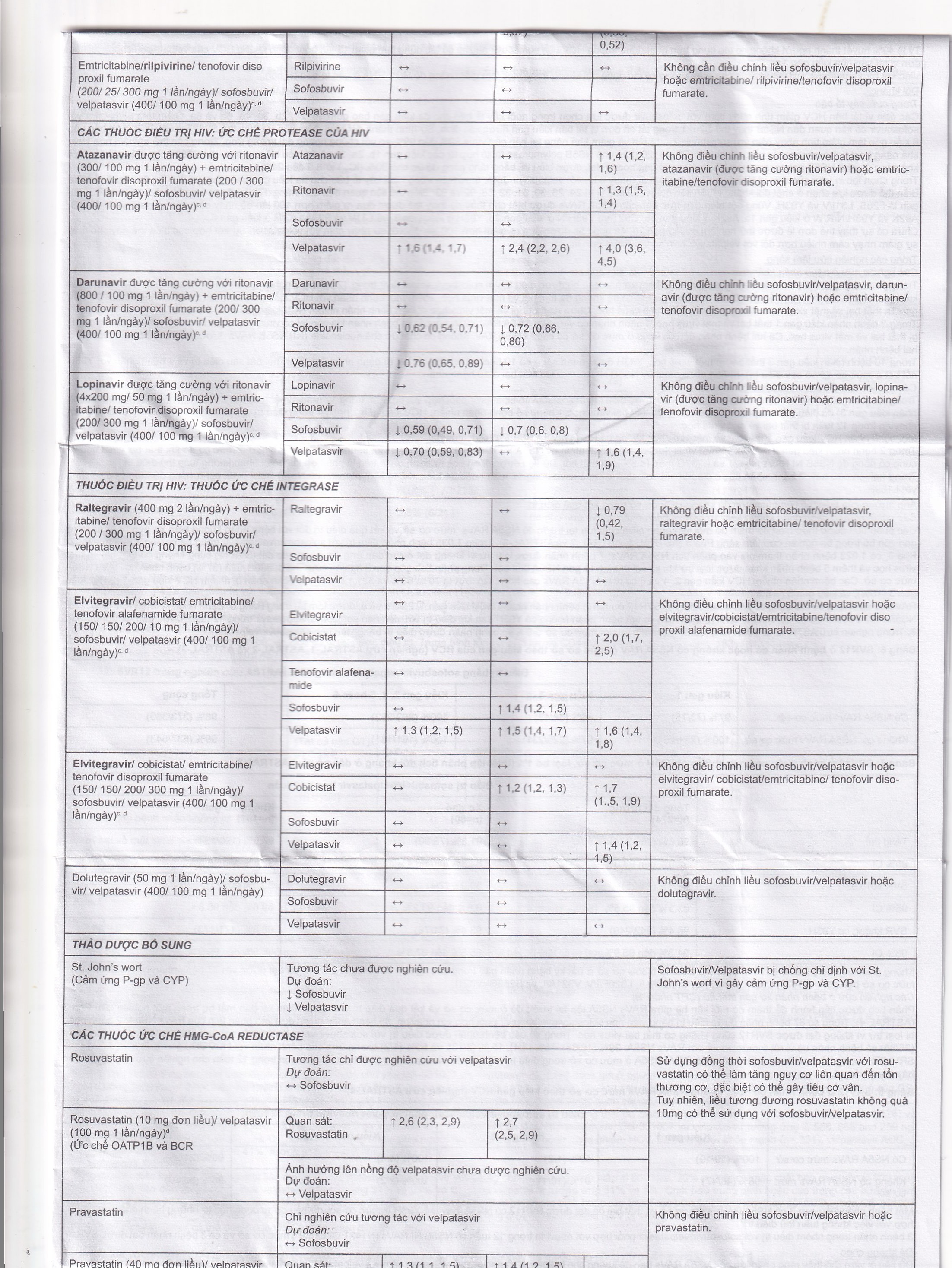
Khả năng in vitro đối với tương tác thuốc thuốc sofosbuvir velpatasvir
Sofosbuvir và velpatasvir là cơ chất của kênh vận chuyển thuốc P-gp và BCRP, trong khi GS-331007 thì không. Velpatasvir cũng là cơ chất của OATP1B. In vitro, quan sát được sự chuyển hóa chậm của of velpatasvir bởi CYP2B6, CYP2C8 và CYP3A4.
Velpatasvir là chất ức chế của kênh vận chuyển thuốc P-gp, BCRP, OATP1B1 và OATP1B3, và sự liên quan của nó trong tương tác thuốc của những chất vận chuyển này là trong giới hạn đầu tiên của quá trình hấp thu. Ở nồng độ huyết tương liên quan lâm sàng, velpatasvir không phải là chất ức chế của chất vận chuyển muối mật ở gan (BSEP), natri taurocholate đồng vận chuyển protein (NTCP), OATP2B1, OATP1A2 hoặc các cation vận chuyển hữu cơ (OCT) 1, các kênh vận chuyển ở thận OCT2, OAT1, OAT3, các protein liên quan đa kháng thuốc 2 (MRP2) hoặc protein kháng đa thuốc và độc tố (MATE) 1 hoặc CYP, hoặc enzyme uridine glucuronosyltransferase (UGT) 1A1.
Sofosbuvir và GS-331007 không phải là chất ức chế của kênh vận chuyển P-gp, BCRP, MRP2, BSEP, OATP1B1, OATP1B3 và OCT1. GS-331007 không phải là chất ức chế của OAT1, OCT2 và MATE1.
Dược động học ở những dân số đặc biệt
Chủng tộc và giới tính
Không có dữ liệu lâm sàng liên quan đến sự khác nhau về được động học của chủng tộc và giới tính với sofosbuvir, GS-331007, hoặc velpatasvir.
Người cao tuổi
Phân tích dược động học dân số ở bệnh nhân viêm gan C cho thấy trong vòng từ 18 đến 82 tuổi, tuổi tác không có ảnh hưởng lâm sàng liên quan đến sofosbuvir, GS-331007, hoặc velpatasvir.
Người suy thận
Dược động học của sofosbuvir đã được nghiên cứu ở những bệnh nhân có HCV âm tính bị suy thận nhẹ (eGFR ≥ 50 và < 80 mL/phút/1,73m2), trung bình (eGFR ≥ 30 và < 50 mL/phút/1,73 m2), suy thận nặng (eGFR <30 mL/phút/1,73 m2) và các bệnh thận ESRD cần chạy thận nhân tạo sau khi uống đơn liều 400 mg sofosbuvir. So với nhóm đối tượng có chức năng thận bình thường eGFR > 80 ml/phút/1,732), AUC0-inf của sofosbuvir cao hơn tương ứng là 61%, 107% và 171% trong các trường hợp suy thận nhẹ, trung bình và nặng, trong khi AUC0-inf của GS-331007 cao hơn tương ứng là 55%, 88% và 451%. Trong các bệnh nhân ESRD, AUC0-inf của sofosbuvir cao hơn 28% khi đã uống liều sofosbuvir 1 giờ trước khi chạy thận nhân tạo, so sánh với cao hơn 60% khi đã uống liều sofosbuvir 1 giờ sau khi chạy thận, tương ứng. AUC0-inf của GS-331007 trong những bệnh nhân ESRD được sử dụng với sofosbuvir 1 giờ trước và 1 giờ sau khi thẩm phân máu ít nhất 10 lần và 20 lần tương ứng. Thẩm phân máu có thể loại bỏ hiệu quả (tỷ lệ thải trừ xấp xỉ 53%) chất chuyển hóa chính GS-331007. Sau khi dùng đơn liều 400 mg sofosbuvir, chạy thận nhân tạo 4 giờ loại bỏ xấp xỉ 18% liều dùng.
Dược động học của velpatasvir đã được nghiên cứu với một liều duy nhất 100 mg velpatasvir ở bệnh nhân HCV âm tính suy thận nặng (eGFR < 30 ml/phút bằng Cockcroft-Gault).
So với các đối tượng có chức năng thận bình thường, velpatasvir AUCinf cao hơn 50% ở những người bị suy thận nặng.
Người suy gan
Dược động học của sofosbuvir đã được nghiên cứu sau 7 ngày dùng liều 400 mg sofosbuvir ở bệnh nhân nhiễm HCV bị suy gan vừa và nặng (CPT nhóm B và C). So với các đối tượng có chức năng gan bình thường, AUC0-24 của sofosbuvir cao hơn 126% và 143%, tương ứng với nhóm đối tượng suy gan vừa và nặng, trong khi AUC0-24 của GS-331007 cao hơn tương ứng là 18% và 9%. Phân tích dược động học dân số trong các bệnh nhân nhiễm HCV chỉ ra rằng xơ gan (bao gồm cả xơ gan mất bù) không có ảnh hưởng liên quan lâm sàng đối với nồng độ của sofosbuvir và GS-331007.
Dược động học của velpatasvir đã được nghiên cứu với một liều duy nhất 100 mg velpatasvir ở bệnh nhân âm tính HCV suy gan vừa và nặng (CPT nhóm B và C). So với các đối tượng có chức năng gan bình thường, tổng nồng độ trong huyết tương (AUCinf) của velpatasvir là tương đương với bệnh nhân suy gan trung bình và nặng. Phân tích dược động học dân số ở những bệnh nhân nhiễm HCV chỉ ra rằng xơ gan (bao gồm cà xơ gan mất bù) không có ảnh hưởng liên quan lâm sàng lên nồng độ của velpatasvir.
Trọng lượng cơ thể
Trọng lượng cơ thể không có ảnh hưởng lâm sàng đáng kể lên nồng độ sofosbuvir hoặc velpatasvir theo phân tích dược động học dân số.
Trẻ em
Dược động học của sofosbuvir, GS-331007 và velpatasvir ở bệnh nhân trẻ em chưa được thiết lập.
Dữ liệu an toàn tiền lâm sàng
Sofosbuvir
Phơi nhiễm với sofosbuvir trong các nghiên cứu với động vật gặm nhấm không thể được phát hiện do hoạt tính esterase cao và phơi nhiễm với các chất chuyển hóa chính GS-331007 được dùng thay thế để dự đoán biên độ phơi nhiễm.
Sofosbuvir không có độc tính gen trong các thử nghiệm in vitro và in vivo, bao gồm đột biến vi khuẩn và đột biến nhiễm sắc thể sử dụng các tế bào lympho ngoại vi ở người và trong các thử nghiệm in vivo đối với chuột nhắt. Không có tác dụng gây quái thai đã được quan sát trong các nghiên cứu phát triển độc tính trên chuột cống và thỏ với sofosbuvir.
Sofosbuvir không có tác dụng không mong muốn đến hành vi, sinh sản, hoặc sự phát triển của con cái trong nghiên cứu phát triển trước và sau sinh ở chuột cống.
Sofosbuvir không phải là một chất gây ung thư trong các nghiên cứu gây ung thư 2 năm ở chuột nhắt và chuột cống ở phơi nhiễm GS-331007 lên tới 15 và 9 lần, tương ứng, cao hơn so với phơi nhiễm ở người.
Velpatasvir
Velpatasvir không có độc tính gen trong các thử nghiệm in vitro và in vivo, bao gồm đột biến vi khuẩn và đột biến nhiễm sắc thể sử dụng các tế bào lympho ngoại vi ở người và trong các thử nghiệm in vivo đối với chuột cống.
Nghiên cứu khả năng gây ung thư với velpatasvir đang được tiến hành.
Velpatasvir không có tác dụng không mong muốn trên giao phối và sinh sản. Không có tác dụng gây quái thai đã được quan sát trong các nghiên cứu phát triển độc tính ở chuột nhắt và chuột cống với velpatasvir tại phơi nhiễm AUC cao hơn xấp xỉ 31 và 6 lần, tương ứng, so với phơi nhiễm ở người tại liều lâm sàng được khuyến cáo. Tuy nhiên, một tác dụng có thể gây quái thai được chỉ ra ở thỏ mà sự gia tăng tổng số dị tật nội tạng đã được nhìn thấy sự phơi nhiễm ở động vật ở phơi nhiễm AUC lên đến 0,7 lần sự phơi nhiễm của con người ở liều lâm sàng được khuyến cáo. Sự liên quan của con người phát hiện này không được biết. Velpatasvir không có tác dụng không mong muốn đến hành vi, sinh sản, hoặc sự phát triển của con cái trong nghiên cứu phát triển trước và sau sinh ở chuột cống tại phơi nhiễm AUC xấp xỉ cao hơn 5 lần so với sự phơi nhiễm ở người ở liều lâm sàng được khuyến cáo.
Cách dùng Thuốc Velsof 400mg/100mg
Cách dùng
Đường uống.
Bệnh nhân uống thuốc nguyên viên kèm theo hoặc không kèm theo thức ăn. Vì thuốc có vị đắng không nên nhai hoặc nghiền nát thuốc.
Liều dùng
Việc điều trị với viên nén sofosbuvir/velpatasvir nên được khởi đầu và theo dõi bởi bác sỹ có kinh nghiệm trong điều trị viêm gan virus C.
Liều khuyến cáo của viên nén sofosbuvir/velpatasvir là uống 1 viên/ngày, kèm hoặc không kèm thức ăn.
| Nhóm bệnh nhâna | Thời gian điều trị |
|---|---|
| Bệnh nhân không xơ gan và bệnh nhân xơ gan còn bù | Uống sofosbuvir/velpatasvir trong 12 tuần Bổ sung ribavirin có thể được xem xét ở bệnh nhân nhiễm kiểu gen 3 với xơ gan còn bù |
| Bệnh nhân xơ gan mất bù | Uống sofosbuvir/velpatasvir + ribavirin trong 12 tuần |
a Bao gồm bệnh nhân đồng nhiễm virus gây suy giảm miễn dịch ở người (HIV) và bệnh nhân tái nhiễm HCV sau khi ghép gan.
Khi sử dụng kết hợp với ribavirin, cũng tham khảo thêm Tóm Tắt Đặc Tính Sản Phẩm của các thuốc có chứa ribavirin.
Mức liều sau đây được khuyến cáo, ribavirin được chia thành 2 lần/ngày, và dùng cùng với thức ăn được trình bày trong bảng 2.
| Bệnh nhân | Liều ribavirin |
|---|---|
| Bệnh nhân xơ gan Child-Pugh-Turcotte (CPT) nhóm B trước khi ghép gan | 1.000 mg/ngày ở bệnh nhân nặng 5 kg và 1.200 mg/ngày ở bệnh nhân nặng ≥ 75 kg. |
Bệnh nhân xơ gan CPT nhóm C trước khi ghép gan Bệnh nhân CPT nhóm B hoặc C sau khi ghép gan | 1.000 mg/ngày ở bệnh nhân nặng 5 kg và 1.200 mg/ngày ở bệnh nhân nặng ≥ 75 kg. Liều khởi đầu 600 mg và điều chim lên đến tối đa 1.000/1.200 mg (1.000mg với bệnh nhân nặng < 75 kg và 1.200 mg ở bên nhà tăng ≥ 75 kg) nếu bệnh nhân có thể dung nạp tốt. Cần giảm liều cho bệnh nên không dung nạp dựa trên nồng độ hemoglobin. |
Nếu sử dụng ribavirin ở bệnh nhân xơ gan còn bù kiểu gen 3 (trước hoặc sau ghép gan), liều khuyến cáo là 1.000 mg/1.200 mg (1.000 mg ở bệnh nhân nặng < 75 kg và 1.200 mg ở bệnh nhân nặng ≥ 75 kg).
Nếu cần thay đổi liều ribavirin, tham khác Tóm Tắt Đặc Tính Sản Phẩm của các thuốc có chứa ribavirin.
Nếu có nôn mùa xảy ra trong vòng 3 giờ sau khi sử dụng thuốc, bệnh nhân cần được hướng dẫn đề uống thêm một viên sofosbuvir/velpatasvir. Nếu nôn mửa xảy ra 3 giờ sau khi dùng thuốc, không cần sử dụng thêm thuốc.
Nếu quên dùng thuốc sofosbuvir/ve patasvir trong vòng 18 giờ kể từ thời gian uống thuốc thông thường bệnh nhân cần được uống bù sớm nhất có thể và tiếp tục uống liều tiếp theo như bình thường. Nếu đã quả 18 giờ không nên uống bù và đợi đến thời gian để uống liều tiếp tục. Khuyến cáo bệnh nhân không uống gấp đôi liều để bù thuốc.
Điều trị bệnh nhân đã điều trị thất bại trước đó với phác đồ có chứa NS5A
Có thể xem xét sử dụng sofosbuvir/velpatasvir kết hợp ribavirin trong 24 tuần.
Người lớn tuổi
Không cần điều chỉnh liều ở người lớn tuổi.
Bệnh nhân suy chức năng thận
Không điều chỉnh liều sofosbuvir/velpatasvir ở bệnh nhân suy chức năng thận mức độ nhẹ và trung bình. Tính an toàn và hiệu quả của sofosbuvirivelpatasvir chưa được đánh giá ở bệnh nhân suy thận mức độ nặng (độ lọc cầu thận ước tính [eGFR] < 30 mL/phút/1,73 m2) hoặc bệnh thận giai đoạn cuối (ESRD) đang chạy thận nhân tạo.
Bệnh nhân suy chức năng gan
Không cần điều chỉnh liều sofosbuvir/velpatasvir ở các bệnh nhân suy gan mức độ nhẹ, trung bình hoặc nặng (CPT nhóm A, B hoặc C). Tính an toàn và hiệu quả của sofosbuvir/velpatasvir đã được đánh giá ở bệnh nhân xơ gan với CPT nhóm B, nhưng chưa được đánh giá trên bệnh nhân xơ gan CPT nhóm C.
Trẻ em
Tính an toàn và hiệu quả của sofosbuvir/velpatasvir ở trẻ em và trẻ vị thành niên dưới 18 tuổi vẫn chưa được thiết lập. Không có dữ liệu sẵn có.
Lưu ý: Liều dùng trên chỉ mang tính chất tham khảo. Liều dùng cụ thể tùy thuộc vào thể trạng và mức độ diễn tiến của bệnh. Để có liều dùng phù hợp, bạn cần tham khảo ý kiến bác sĩ hoặc chuyên viên y tế.
Làm gì khi dùng quá liều?
Liều cao nhất của sofosbuvir và velpatasvir đã được sử dụng lần lượt là liều đơn 1200 mg và 500 mg. Trong các nghiên cứu ở người tình nguyện khỏe mạnh, chưa có tác dụng không mong muốn nào được quan sát thấy ở các mức liều nói trên, và tác dụng không mong muốn có tần số và mức độ nghiêm trọng là tương tự với các tác dụng không mong muốn được quan sát ở bệnh nhân sử dụng giả dược. Hiện chưa rõ tác dụng của thuốc khi sử dụng liều cao.
Hiện chưa có thuốc giải độc đặc hiệu dùng cho trường hợp sử dụng quá liều sofosbuvir/velpatasvir. Điều trị quá liều với sofosbuvir/velpatasvir gồm các biện pháp hỗ trợ chung bao gồm theo dõi dấu hiệu sống còn, cũng như quan sát tình trạng lâm sàng của bệnh nhân. Thẩm phân tách máu có thể loại bỏ một cách hiệu quả chất chuyển hóa chính đang lưu thông của sofosbuvir, GS-331007, với tỷ lệ thải trừ là 53%. Thẩm phân tách máu dường như không loại bỏ đáng kể velpatasvir do velpatasvir liên kết mạnh với protein huyết tương.
Trong trường hợp khẩn cấp, hãy gọi ngay cho Trung tâm cấp cứu 115 hoặc đến trạm Y tế địa phương gần nhất.
Làm gì khi quên 1 liều?
Bổ sung liều ngay khi nhớ ra. Tuy nhiên, nếu thời gian giãn cách với liều tiếp theo quá ngắn thì bỏ qua liều đã quên và tiếp tục lịch dùng thuốc. Không dùng liều gấp đôi để bù cho liều đã bị bỏ lỡ.
Tác dụng phụ
Khi sử dụng thuốc Velsof bạn có thể gặp các tác dụng không mong muốn (ADR):
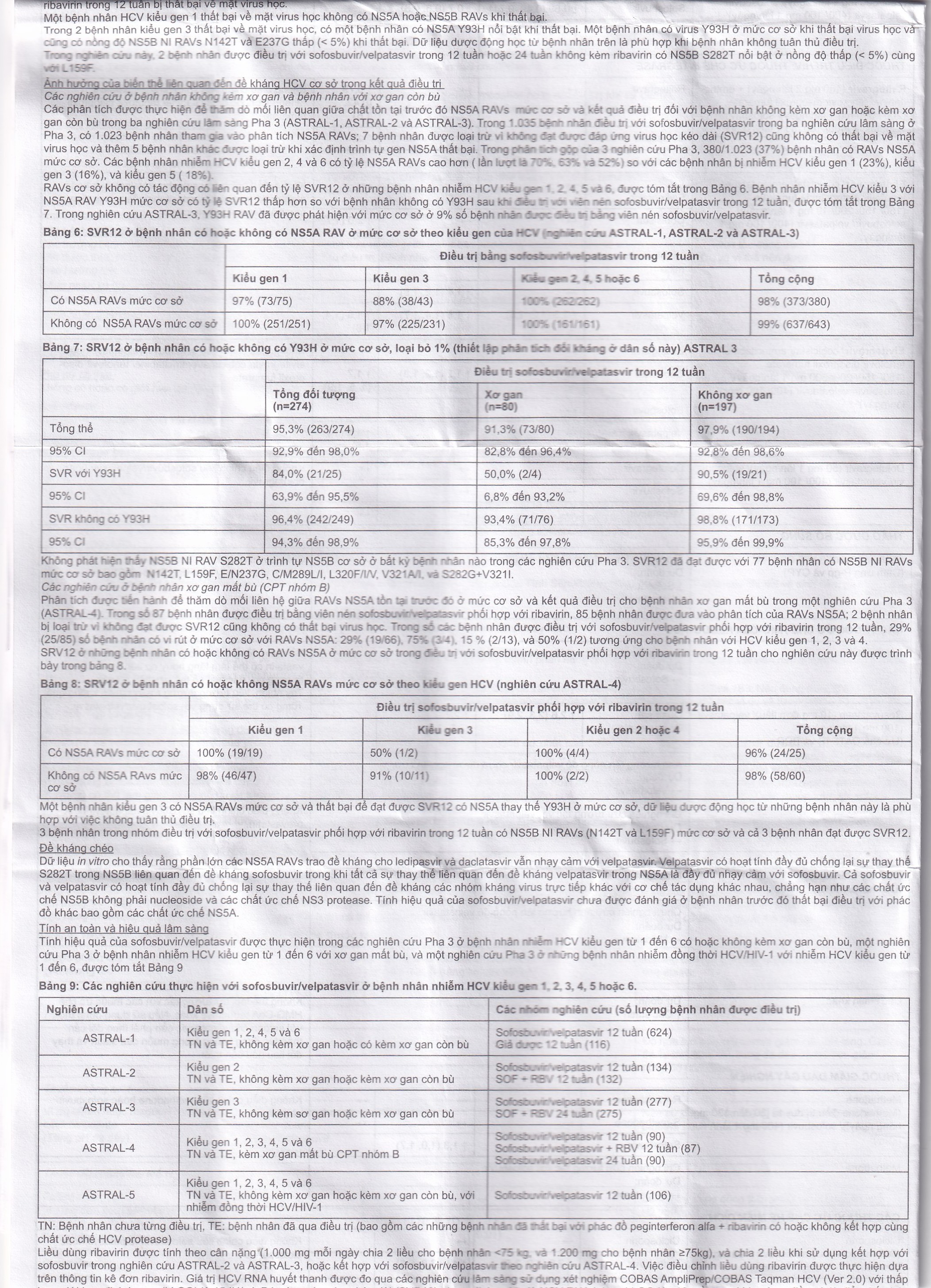
Tóm tắt sơ lược tính an toàn
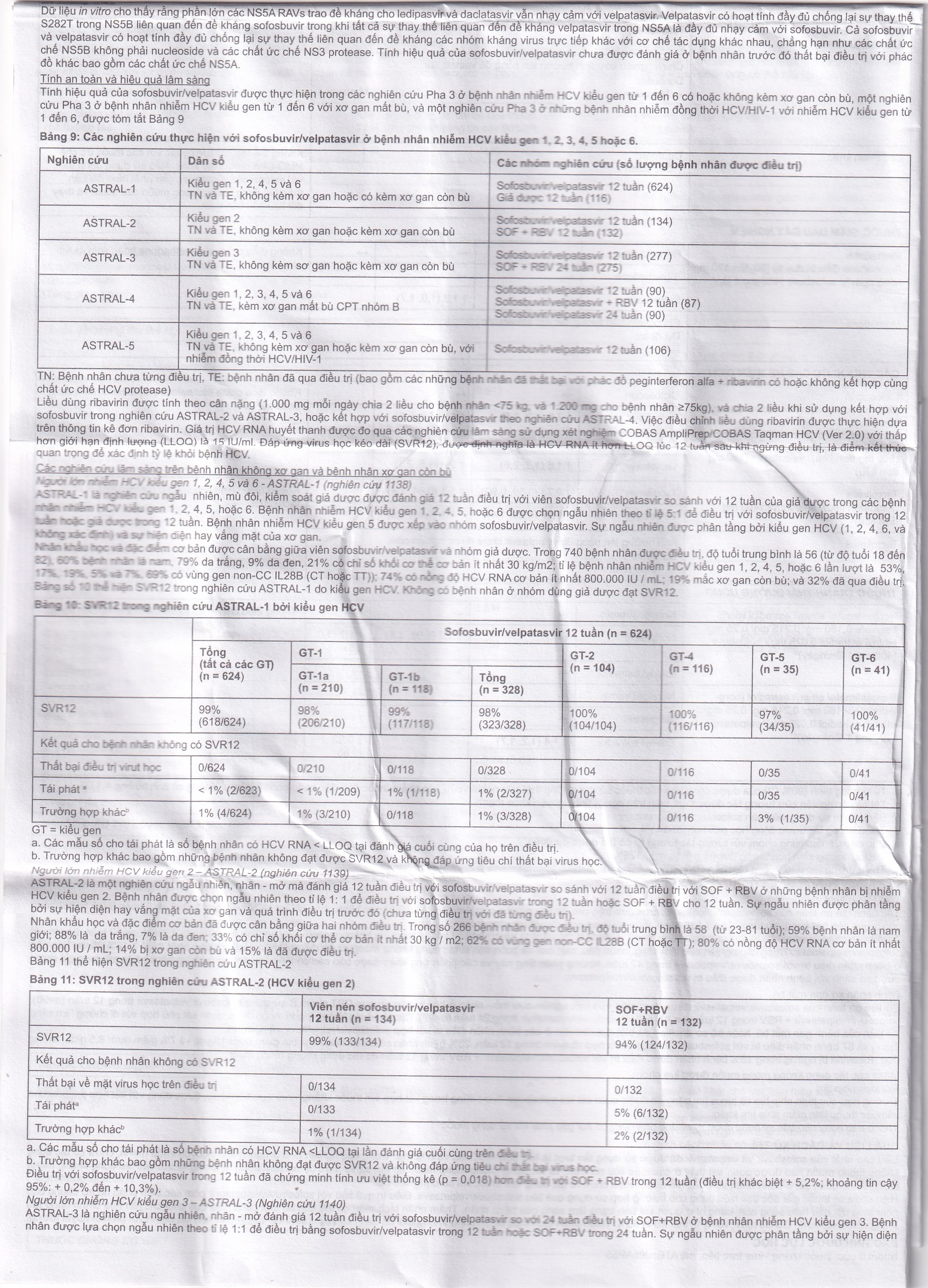
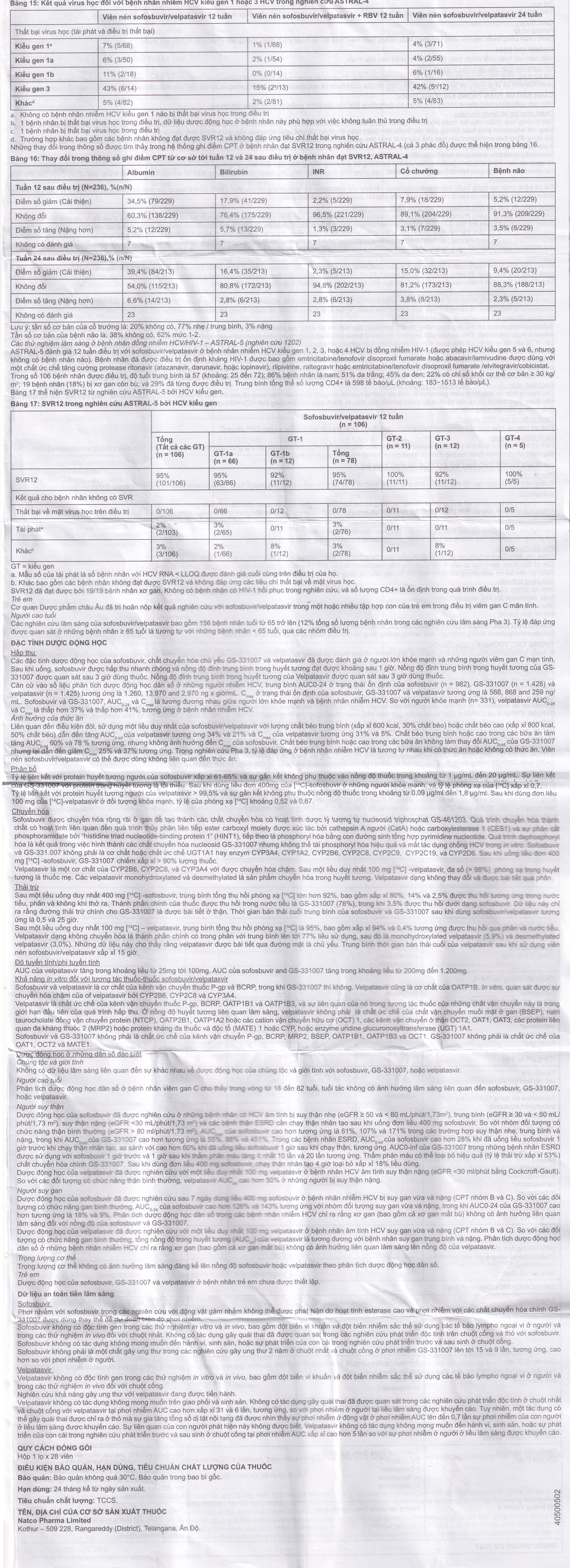
Các đánh giá an toàn của sofosbuvir/velpatasvir được dựa trên các dữ liệu nghiên cứu lâm sàng Pha 3 từ các bệnh nhân nhiễm HCV kiểu gen 1, 2, 3, 4, 5 hoặc 6 (có hoặc không có xơ gan còn bù) bao gồm tổng cộng 1.035 bệnh nhân sử dụng sofosbuvir/velpatasvir trong 12 tuần.
Tỷ lệ bệnh nhân ngưng điều trị do tác dụng không mong muốn là 0,2% và tỷ lệ bệnh nhân có bất kỳ tác dụng không mong muốn nghiêm trọng nào là 3,2% trong 12 tuần điều trị với sofosbuvir/velpatasvir. Trong các nghiên cứu lâm sàng, nhức đầu, mệt mỏi và buồn nôn là tác dụng không mong muốn điều trị khẩn cấp phổ biến nhất (tỷ lệ ≥ 10%) được báo cáo ở bệnh nhân điều trị với sofosbuvir/velpatasvir trong 12 tuần. Những phản ứng này và các phản ứng khác được báo cáo có tần số tương tự ở nhóm bệnh nhân sử dụng giả được được so sánh với bệnh nhân được điều trị với sofosbuvir/velpatasvir.
Bệnh nhân xơ gan mất bù
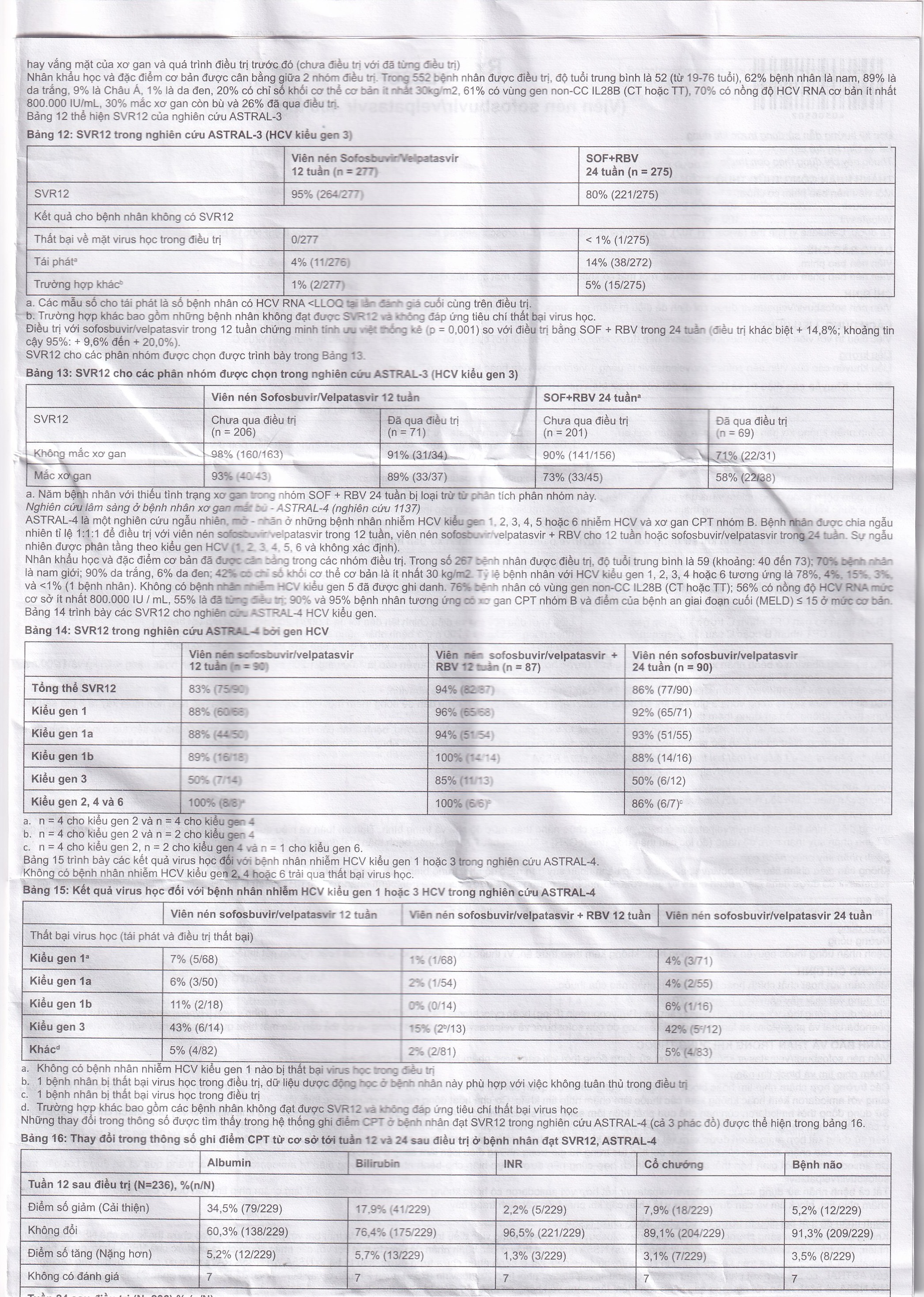
Dữ liệu an toàn của sofosbuvir/velpatasvir được thực hiện trên một nghiên cứu mở - nhân ở bệnh nhân xơ gan CPT nhóm B sử dụng sofosbuvir/velpatasvir trong 12 tuần (n=90), sofosbuvir/velpatasvir + RBV trong 12 tuần (n=87) hoặc sofosbuvir/velpatasvir trong 24 tuần (n=90). Các tác dụng không mong muốn được quan sát phù hợp với di chứng lâm sàng dự kiến của bệnh gan mất bù, hoặc hồ sơ độc tính đã biết của ribavirin ở các bệnh nhân điều trị kết hợp sofosbuvir/velpatasvir và ribavirin.
Trong số 87 bệnh nhân điều trị với sofosbuvir/velpatasvir kết hợp ribavirin trong 12 tuần, 23% bệnh nhân có chỉ số haemoglobin giảm dưới 10g/dL và 7% giảm dưới 8,5 g/dL, tương ứng. Ribavirin bị ngừng trong 15% bệnh nhân được điều trị với sofosbuvir/velpatasvir + RBV trong 12 tuần do tác dụng không mong muốn.
Mô tả các tác dụng không mong muốn được lựa chọn
Rối loạn nhịp tim
Trường hợp của loạn nhịp tim và block tim nặng đã được quan sát khi sofosbuvir được dùng trong kết hợp với thuốc kháng virus trực tiếp khác, được dùng với kết hợp amiodarone và/hoặc thuốc làm giảm nhịp tim khác.
Hướng dẫn cách xử trí ADR:
Thông báo cho thầy thuốc các tác dụng không mong muốn gặp phải khi sử dụng thuốc.
Bảo quản
Hạn sử dụng: 24 tháng
Bảo quản nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp.
Để xa tầm tay trẻ em.